吉林大学分子酶学工程教育部重点实验室的王磊教授课题组致力于研究利用人工酶挖掘新型非天然反应,以实现绿色高效的有机合成。通过设计全新的人工金属酶,以《Enzyme-Controlled Bidirectional Enantioselectivity in Asymmetric Decarboxylative Mannich Reaction for Synthesizing β-Sulfonamide Ketones》为题在国际期刊ACS Catalysis发表研究论文。
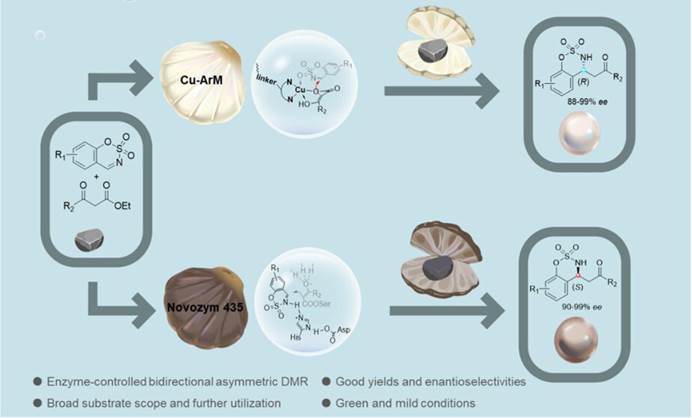
该研究报道了一种酶控双向对映选择性催化策略,用于不对称脱羧曼尼希反应(DMR)合成手性β-磺酰胺酮。研究通过构建铜人工金属酶(Cu-ArM)和利用商业脂肪酶Novozym 435,分别实现对R和S构型产物的高选择性合成。Cu-ArM由生物素化铜复合物与链霉亲和素(WT-Sav)组装而成,催化环状磺酰胺与β-酮酯反应生成R构型产物;而Novozym 435通过其催化三元活性中心调控反应路径,高效获得S构型产物。分子动力学模拟揭示了酶-底物相互作用机制,阐明环状亚胺因稳定氢键网络和紧凑构象而优于非环状底物的原因。该方法在温和水相条件下实现低催化剂负载(Cu-ArM仅0.5 mol%),并成功应用于克级合成及药物分子衍生物制备(如降压抗炎活性分子chroman-4-amine)。该工作为绿色合成手性含氮药物分子提供了新范例,拓展了生物催化在不对称合成中的应用潜力。论文第一完成单位为吉林大学生命科学学院,吉林大学生命科学学院博士研究生唐勇和许雅宁博士为该论文的共同第一作者,吉林大学王磊教授,李奉熙博士为该论文的共同通讯作者。
论文链接:https://pubs.acs.org/doi/10.1021/acscatal.4c06927