HIV-1是导致获得性免疫缺陷综合征(AIDS)的主要病原体,其可利用宿主细胞糖基化等途径来加工病毒包膜蛋白(Env),Env表面的糖链能够遮蔽抗原表位,保护蛋白质免受免疫监视,被称之为“糖盾”。研究发现Env的糖基化修饰有着高度保守的结构,被视为抑制 HIV-1 感染的重要突破口之一,但由于免疫原性较弱,针对病毒糖链的抗体难以获得,且现有靶向Env糖链的中和抗体存在半衰期短和易于引发逃逸突变等缺点。分子印迹(Molecular Imprinting)技术通过模板分子空间结构和结合位点来模拟抗原-抗体之间的相互作用,从而精确识别目标分子。分子印迹材料有着卓越的分子识别性能和稳定性,被称之为人工抗体,已被广泛应用于色谱分离、生物传感、药物递送和仿生催化等诸多领域。基于此,吉林大学于湘晖教授/胡良海教授团队和中科院大连化物所叶明亮研究员团队合作,开发了针对 HIV-1表面蛋白"糖盾"的分子印迹人工抗体材料,从而有效抑制病毒对细胞的感染,相关研究内容以“Glycan Imprinted Nanoparticle as Artificial Neutralizing Antibody for Efficient HIV-1 Recognition and Inhibition”为题在Nano Letters在线发表。

本研究以生物相容性较高的SiO2为内核,以HIV-1病毒糖链分子为模板,以可与糖链上的顺式二羟基进行可逆共价反应的硼酸基团为功能单体,制备了分子印迹纳米微球。体外实验结果显示所制备的分子印迹材料对HIV-1病毒颗粒具有媲美抗体的选择性和结合力,且可抵抗血浆等复杂基质的干扰,为其在真实环境中的应用提供了保障。针对于HIV-1病毒表面糖链的定量蛋白质组学的分析揭示了Env糖链结构的序列特异性,是良好的结合靶点。竞争性结合实验结果进一步表明了Env糖链是印迹空腔的亲和作用位点,从而通过阻断Env蛋白与宿主细胞受体CD4的结合来抑制病毒的复制与感染。细胞水平抗感染实验结果显示该印迹材料对HIV-1一级(tier 1)毒株和难以被天然抗体中和的二级(tier 2)毒株均表现出良好的中和效果;同时对病毒长期复制的抑制效果也非常显著,在9天内可以将HIV-1的病毒载量控制在对照组的1%以下,有效控制了病毒的复制。靶向糖链的分子印迹人工中和抗体为HIV-1的纳米治疗提供了新的解决方案,有着广阔的应用前景。
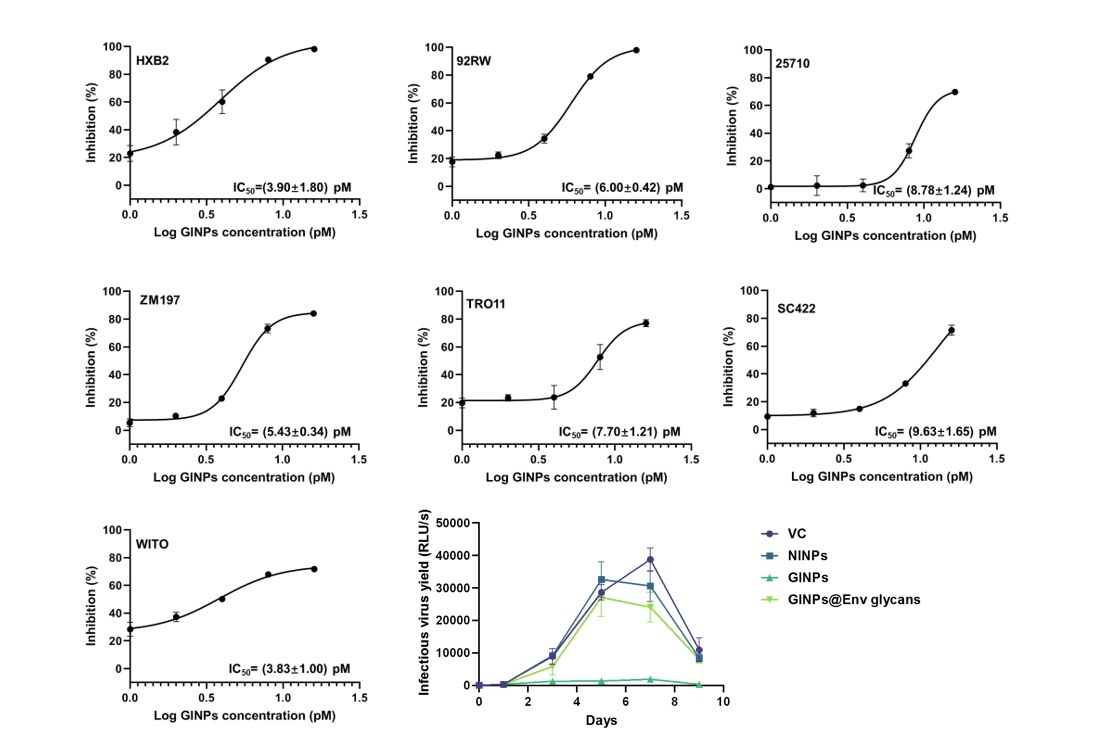
分子印迹人工抗体对不同亚型毒株的抗感染IC50和长期抑制曲线
吉林大学博士研究生周俊涛、王莉变和大连化物所博士研究生刘晓艳为论文的共同第一作者,吉林大学于湘晖教授和胡良海教授为论文的共同通讯作者。本研究得到了国家重点研发计划、国家自然科学基金和南京大学生命分析化学国家重点实验室开放课题的支持,实验设计与论文撰写过程中得到了南京大学刘震教授团队的指导和帮助。
全文链接:https://doi.org/10.1021/acs.nanolett.4c00142